Después de ‘construir’ máquinas vivas a partir de células reutilizadas de embriones de rana, un grupo de científicos de EE UU ha creado los primeros biobots capaces de reproducirse de una manera jamás observada antes en el mundo animal o vegetal. Esta nueva forma de autorreplicación biológica podría suponer un prometedor avance para la medicina regenerativa.
Mitad animal, mitad robot. Los xenobots, creados gracias a la reutilización de células vivas obtenidas de embriones de rana de uñas africanas (Xenopus laevis), fueron diseñados en una supercomputadora a partir de bloques de construcción biológicos específicos basados en un algoritmo evolutivo.
Estos biobots, creados por un grupo de jóvenes investigadores estadounidenses, fueron dados a conocer en 2020. En ese momento, medían un milímetro de largo, eran capaces de moverse hacia un objetivo marcado, levantar carga útil o autocurarse tras un corte.
Ahora, en un nuevo estudio publicado en la revista PNAS, los cuatro científicos presentan los primeros robots vivos autorreplicantes de la historia, gracias al hallazgo de una nueva forma de reproducción biológica. Los autores extrajeron células cutáneas no modificadas genéticamente de renacuajos de Xenopus y las incubaron para producir organismos móviles y multicelulares cubiertos de cilios (estructuras celulares con aspecto de pestaña).
Estos biobots, diseñados por ordenador y ensamblados a mano, pueden nadar en una placa Petri, encontrar células individuales y reunir cientos de ellas y juntar ‘bebés’ xenobot en el interior de su boca en forma de Pac-Man.
Unos cinco días más tarde, estos se convierten en nuevas máquinas vivas, que pueden observarse y moverse de la misma manera. A su vez, encuentran células y construyen copias de sí mismos, una y otra vez. “Con el diseño adecuado, se autorreplican espontáneamente”, afirma Joshua Bongard, informático y experto en robótica de la Universidad de Vermont (UVM), que ha codirigido el trabajo.
Las células embrionarias de rana empleadas para crear los xenobots estaban así destinadas para convertirse en piel. Situadas en el exterior del renacuajo, su función sería la de mantener a los patógenos alejados y redistribuir la mucosidad. En el estudio, los investigadores las colocaron en otro contexto completamente novedoso.
“Les dimos la oportunidad de reimaginar su multicelularidad”, señala Michael Levin, profesor de biología y director del Allen Discovery Center de la Universidad de Tufts y colíder del trabajo. Y lo que imaginan es algo muy diferente a la piel.
“Estas células tienen el genoma de una rana, pero, liberadas de convertirse en renacuajos, utilizan su inteligencia colectiva, una plasticidad, para hacer algo asombroso”, añade Levin. Nunca antes se había observado una manera de reproducción así en un animal o una planta.
Según Sam Kriegman, autor principal, y ahora investigador postdoctoral en el Centro Allen de Tufts y el Instituto Wyss de la Universidad de Harvard, se trata de células de rana que se replican de una forma muy diferente a como lo hacen estos anfibios.
Por sí solo, el progenitor xenobot, compuesto por unas 3.000 células, forma una esfera. “Estas pueden hacer hijos, pero después el sistema normalmente se extingue. En realidad, es muy difícil conseguir que el sistema siga reproduciéndose”, dice Kriegman.

Pedimos al superordenador de la UVM que averiguara cómo ajustar la forma de los progenitores iniciales, y la IA dio con algunos diseños extraños tras meses de trabajo, incluido uno que se parecía a Pac-Man

Pero gracias a un programa de inteligencia artificial (IA) del clúster de supercomputación Deep Green del Vermont Advanced Computing Core de la UVM, un algoritmo evolutivo probó miles de millones de formas corporales en simulación (triángulos, cuadrados, pirámides, estrellas de mar, etc.) para encontrar las que permitían a las células ser más efectivas en la replicación “cinemática” basada en el movimiento, que nunca antes se había observado a escala de células u organismos enteros.
“Pedimos al superordenador de la UVM que averiguara cómo ajustar la forma de los progenitores iniciales, y la IA dio con algunos diseños extraños tras meses de trabajo, incluido uno que se parecía a Pac-Man”, cuenta Kriegman.
Aunque los investigadores se extrañaron de la forma de la boca –poco intuitiva, pequeña y única–, enviaron los resultados a Douglas Blackiston, el científico principal de la Universidad de Tufts que reunió a los ‘padres’ Xenobot con forma de Pac-Man y desarrolló la parte biológica del nuevo estudio. A partir de ahí, los biobots crearon hijos, nietos, bisnietos y tataranietos, ampliando el número de generaciones.
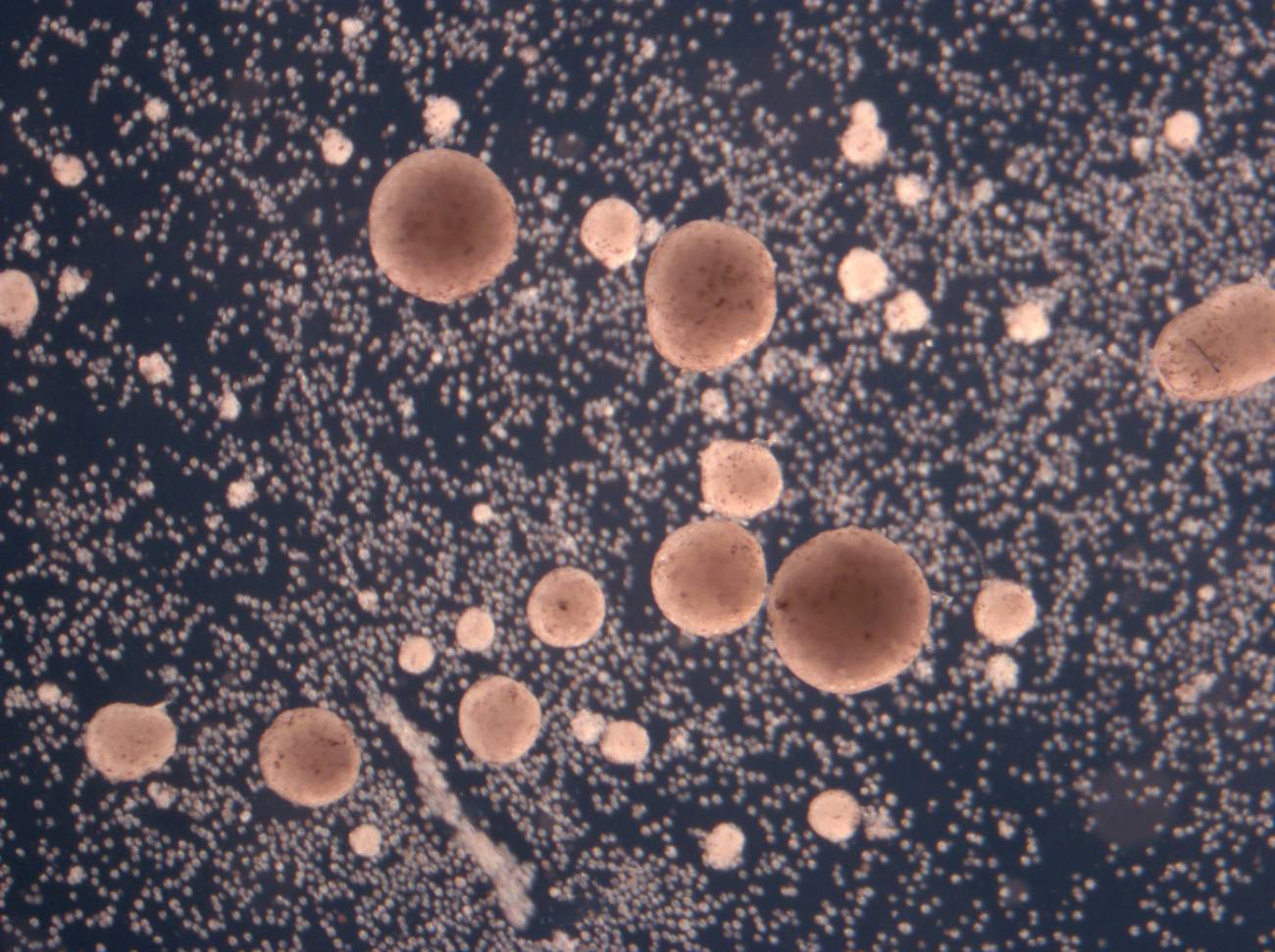
Descendencia de los xenobots: células madre compactadas en esferas por ‘padres’ diseñados por IA. / Douglas Blackiston & Sam Kriegman
Según los autores, la creación de estas máquinas vivientes supone trabajar más profundidad en la comprensión de la replicación: “El mundo y las tecnologías están cambiando rápidamente. Es importante, para la sociedad en su conjunto, que estudiemos y entendamos cómo funciona”, informa Bongard.
Estas máquinas vivientes de tamaño milimétrico, creadas por completo en laboratorio, fácilmente extinguibles y examinadas por expertos, se convierten en el sistema ideal para estudiar los sistemas autorreplicantes. “Tenemos el imperativo moral de comprender las condiciones en las que podemos controlarlo, dirigirlo, apagarlo o exagerarlo”, recalcan.
Para los científicos, esta investigación es prometedora para los avances hacia la medicina regenerativa. “Si supiéramos cómo decirle a los grupos de células que hagan lo que queremos que hagan, sería la solución a las lesiones traumáticas, los defectos de nacimiento, el cáncer y el envejecimiento”, apunta Levin, para quien estos problemas existen porque no sabemos cómo predecir y controlar qué grupos de células van a construir. “Los xenobots son una nueva plataforma para enseñarnos”, concluye.
Referencia:
Sam Kriegman et al. “Kinematic self-replication in reconfigurable organisms” PNAS