La investigadora francesa Emmanuelle Charpentier y la estadounidense Jennifer A. Doudna han sido galardonadas con el Premio Nobel de Química 2020 por el desarrollo de un método para editar el genoma: CRISPR/Cas9, una herramienta para reescribir el código de la vida que puede hacer realidad el sueño de curar enfermedades hereditarias.
La Academia Sueca de las Ciencias ha anunciado hoy que el Premio Nobel de Química de este año ha recaído en las investigadoras Emmanuelle Charpentier de la Unidad Max Planck para la Ciencia de los Patógenos (Alemania) y Jennifer A. Doudna de la Universidad de California en Berkeley (EE UU).
“Este premio trata sobre la reescritura del código de la vida”, ha subrayado Goran K. Hansson, secretario general de la Academia, al anunciar los nombres de las laureadas.
Charpentier (Juvisy-sur-Orge-Francia, 1968) y Doudna (Washington-EE UU, 1964) han descubierto una de las herramientas más afinadas de la tecnología genética: las tijeras genéticas CRISPR/Cas9.
Con estas tijeras, los investigadores pueden cambiar el ADN de animales, plantas y microorganismos con una precisión extremadamente alta. Esta tecnología ha tenido un impacto revolucionario en las ciencias de la vida, está contribuyendo a nuevas terapias contra el cáncer y puede hacer realidad el sueño de curar enfermedades hereditarias.
Los científicos necesitan modificar los genes en las células si quieren descubrir el funcionamiento interno de la vida. Esto solía ser un trabajo lento, difícil y, a veces, imposible. Pero usando las tijeras genéticas CRISPR / Cas9, ahora es posible cambiar el código de la vida en el transcurso de unas pocas semanas.
“Hay un poder enorme en esta herramienta genética, que nos afecta a todos. No solo ha revolucionado la ciencia básica, sino que también ha dado lugar a cultivos innovadores y dará lugar a nuevos tratamientos médicos innovadores”, ha subrayado Claes Gustafsson, presidente del Comité Nobel de Química.
Como suele ocurrir a mendo en la ciencia, el descubrimiento de estas tijeras genéticas fue inesperado. Durante los estudios de Charpentier sobre Streptococcus pyogenes, una de las bacterias que más daño causan a la humanidad, encontró una molécula previamente desconocida, el ARNtracr (o ARNcr trans-activado). Su trabajo mostró que este ARN es parte del antiguo sistema inmunológico de las bacterias, CRISPR/Cas, que desarma los virus al escindir su ADN.
El científico español Francis Mojica de la Universidad de Alicante fue el que introdujo el término CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats, repeticiones palindrómicas cortas agrupadas y regularmente espaciadas) y describió en los años 90 las secuencias repetidas CRISPR en arqueas de las salinas de Santa Pola.
Más tarde descubrió que secuencias similares estaban muy extendidas en los organismos procariotas y coincidían con el material genético de los fagos, virus que infectan bacterias, planteando que esas repeticiones eran parte de un sistema inmunológico microbiano.
“No habría CRISPR sin Francisco Mojica”, destaca en un artículo la revista Nature, la misma que en 2003 rechazó el estudio del microbiólogo español donde presentaba sus descubrimientos.
Pero Charpentier fue más allá con el hallazgo del ARNtracr y publicó su descubrimiento en 2011. El mismo año, inició una colaboración con Jennifer Doudna, una bioquímica experimentada con un vasto conocimiento del ARN. Juntas, lograron recrear las tijeras genéticas de las bacterias en un tubo de ensayo y simplificaron sus componentes moleculares para que fueran más fáciles de usar.
En un experimento que hizo historia, lograron reprogramar las tijeras genéticas. En su forma natural, estas reconocen el ADN de los virus, pero Charpentier y Doudna demostraron que podían controlarse para cortar cualquier molécula de ADN en un sitio predeterminado. Y donde se corta el ADN, es fácil reescribir el código de la vida.
Desde que Charpentier y Doudna crearon las tijeras genéticas CRISPR/Cas9 en 2012, su uso se ha disparado. Esta herramienta ha contribuido a muchos descubrimientos importantes en la investigación básica, y los científicos que trabajan con plantas han podido desarrollar cultivos que resisten el moho, las plagas y la sequía.
En medicina, ya se están realizando ensayos clínicos relacionados con terapias innovadoras contra el cáncer, y la posibilidad de curar enfermedades hereditarias cada vez está más cerca de hacerse realidad. Estas tijeras genéticas han llevado las ciencias de la vida a una nueva época y han comenzado a aportar enormes beneficios para la humanidad.
En el más de un siglo de historia de los Premios Nobel es la primera vez que dos mujeres comparten el de Química, aunque Marie Curie ya lo recibió sola en 1911. El mismo galardón lo ganaron luego su hija Irène Joliot-Curie (1935), Dorothy Crowfoot Hodgkin (1964), Ada Yonath (2009) y Frances Arnold (2018).
“Mi deseo es que este premio aporte un mensaje positivo a las jóvenes que deseen seguir el camino de la ciencia, y muestre que las mujeres también pueden tener un impacto a través de la investigación que están realizando”, ha declarado Charpentier.
Por su parte Doudna, a la que sorprendió dormida el anuncio del Nobel, ha destacado que este premio "reconoce la historia colaborativa de CRISPR y su aprovechamiento en una tecnología poderosa que brinda nuevas esperanzas y posibilidades a nuestra sociedad”.
“Lo que comenzó como un proyecto de descubrimiento fundamental impulsado por la curiosidad –ha recordado–, ahora se ha convertido en una estrategia innovadora utilizada por innumerables investigadores que trabajan para ayudar a mejorar la condición humana. Yo animo a continuar apoyando la ciencia básica, así como el discurso público sobre los usos éticos y la regulación responsable de la tecnología CRISPR".
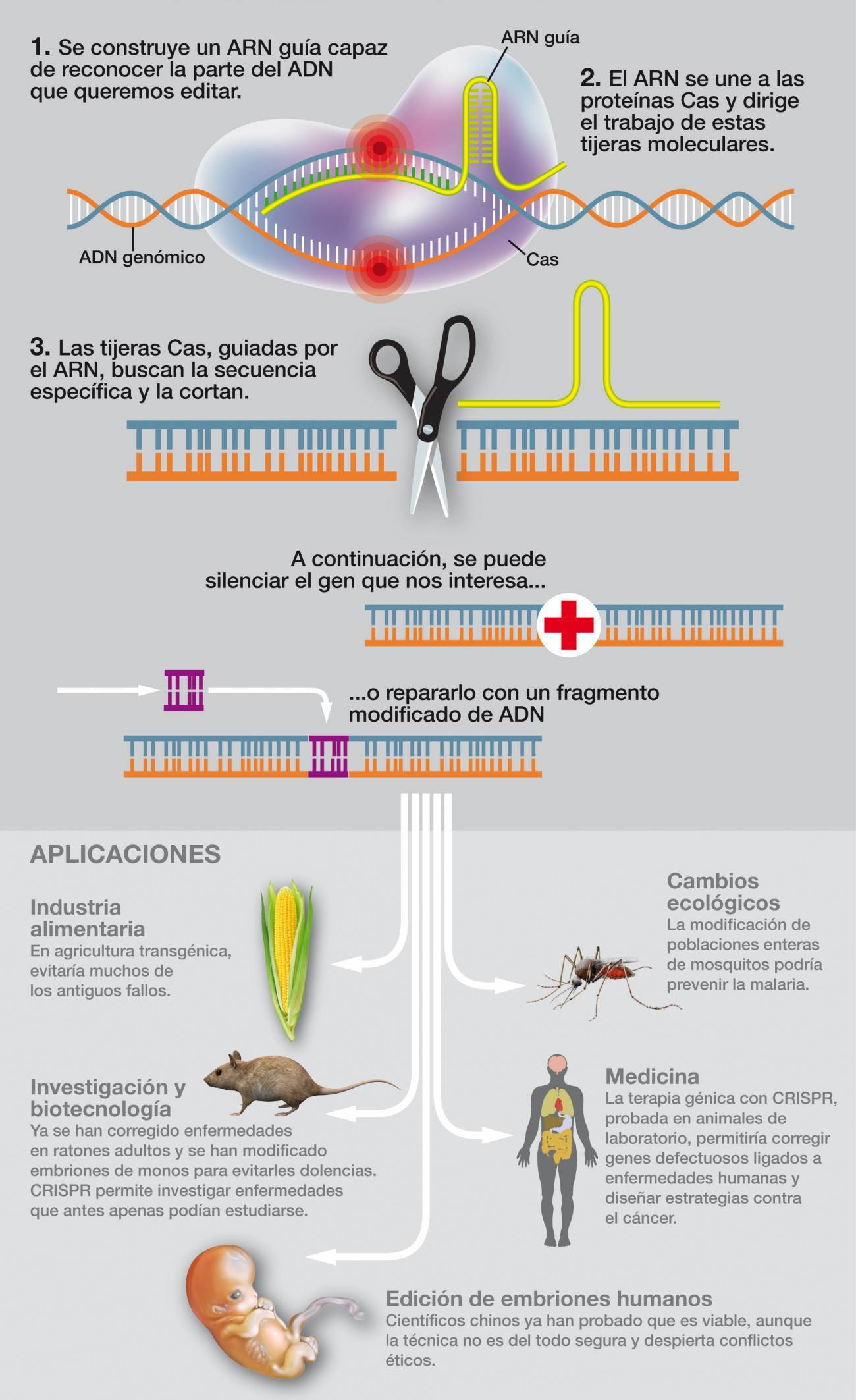
Así funciona CRISPR, la revolucionaria herramienta de edición de ADN. / José Antonio Peñas/SINC